| wcg112233 | 2019-12-25 08:29 |
|
糖尿病是一组以高血糖为特征的代谢性疾病,已经成为危害人类健康的“第三大杀手”。 按胰岛素分泌的情况,糖尿病可分为1型和2型,2型糖尿病与胰岛素抵抗和胰岛β细胞功能缺陷有关,且多见于成人。据统计,中国2型糖尿病的患病率达11.6%,而糖尿病前期人群更是高达 50.1%。 也就是说2个成人里就有1个是“糖尿病”的“后备军”。 在糖尿病研究中,一个核心问题是,为什么β细胞最初会分泌过多的胰岛素。 通俗的说法是,此时人体可能感知不到胰岛素的存在,因此β细胞会分泌更多胰岛素来引起人体的“注意”。 但让人困惑的是,即使是实验室培养皿中分离出的β细胞也会过度分泌胰岛素。 一项刊发于美国《Diabetes》杂志的新研究提出了一种专门调节胰岛中非葡萄糖刺激的胰岛素分泌(NGSIS)的机制,该机制由非酯化的游离脂肪酸(禁食期间β细胞利用的主要燃料)激活。  https://doi.org/10.2337/db19-0379 在实验过程中,科学家以普通小鼠和糖尿病前期小鼠为对象,对机体在没有葡萄糖的情况下分泌胰岛素的机制进行了研究。 结果发现,在糖尿病前期小鼠的β细胞中,线粒体通透性转换孔调节因子环亲素D(CypD)通过增加线粒体质子泄漏,能够在葡萄糖没有升高的情况下促进胰岛素的分泌。 与瘦小鼠相比,糖尿病前肥胖小鼠的胰岛显示出明显更高的CypD依赖性质子泄漏和NGSIS。 其机制依赖于脂肪酸,而脂肪酸通常不能刺激健康动物的胰岛素分泌。 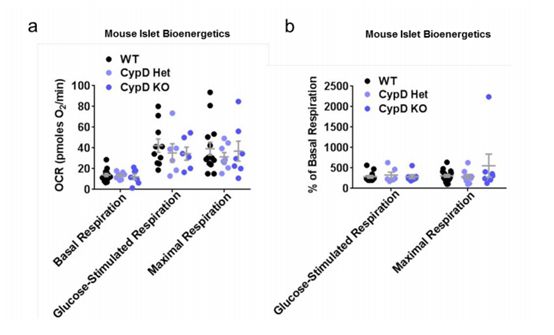 另外,缺乏CypD基因的肥胖小鼠不会分泌过量的胰岛素。 实验过程中,研究人员观察到,NGSIS也发生在分离的人类胰腺细胞中: 当脂肪酸水平达到肥胖群体的典型水平时,细胞能够在没有葡萄糖升高的情况下分泌胰岛素。 总之,这项研究揭示了选择性驱动胰岛NGSIS的非酯化游离脂肪酸刺激途径,同时也为我们提供了预防胰岛素抵抗和治疗糖尿病的新方法,包括通过阻止β细胞质子泄漏来阻止其进展。 |
|